国家卫健委:86种罕见病纳入目录部分病种政策不断发力
2023-09-22 12:10:13 來源: 搜虎网

罕见病领域再次迎来政策利好。
9月20日,国家卫健委官网公布了科技部、工业和信息化部、国家食品药品监督管理局、国家总局联合制定的《第二批罕见病目录》中医药管理局、中央军委后勤保障部. 共纳入86种罕见病。 加上2018年5月五部门发布的《第一批罕见病目录》,目前目录已涵盖207种罕见病。
9月21日,澎湃新闻记者发现,多家A股及港股上市公司的产品适应症均被纳入上述目录中。 多位业内人士向澎湃新闻记者指出,目录的扩大意味着国家层面对罕见病更加重视。 进入国家罕见病目录后,有望加快相关产品的审批进度,加快产品上市时间,让更多罕见病得以释放。 患者受益。

第二批罕见病目录中的部分疾病
政策持续聚焦罕见病领域
《第二批罕见病目录》的出台并不突然。 早在今年1月,国家卫健委官网发布的《关于加大罕见病诊疗投入的建议》的回复中就提到,国家卫健委将按照配合罕见病目录,及时调整更新第二批罕见病目录。
罕见病又称孤儿病,是指发病率极低、受影响人群极少数的疾病。 其特点是类型多,以遗传为主,诊断困难、病情重、可治性低、治疗费用高。 目前,全球已发现7000多种罕见病,但只有10%的罕见病有相应的治疗方法。
为解决罕见病问题,相关部门正在多方面努力。

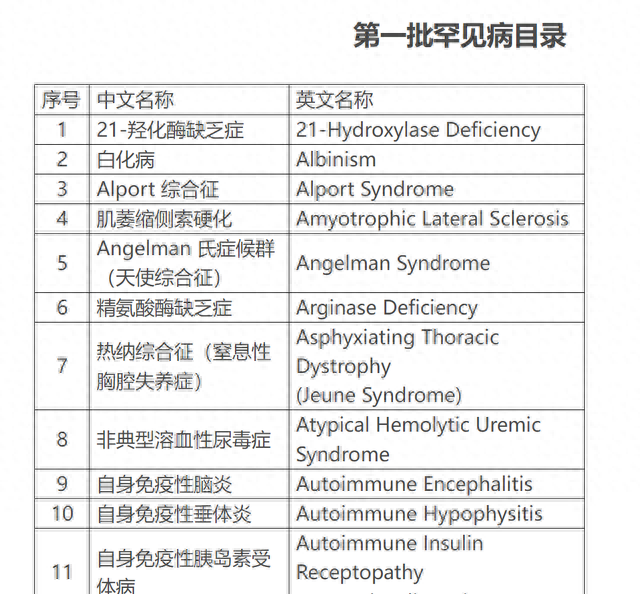
第一批罕见病目录中的部分疾病
2019年,结合《第一批罕见病目录》发布,国家卫健委制定发布了《罕见病诊疗指南》,明确了包括的121种疾病的诊疗指南对罕见病管理一一进行,并依托行业组织对医务人员进行培训。 、提高罕见病规范诊疗能力。 同时,依托国家罕见病诊疗协作网络办公室,在协作网络医院之间开展医师培训,提高医生诊治罕见病的能力。
药物批准也有利于治疗罕见疾病的药物。 2020年3月发布的《药品注册管理办法》指出,临床急需的已在境外上市但尚未在境内上市的罕见病药品,审评时限为70天。 2022年5月,《药品管理法实施条例(修订草案征求意见稿)》提出,罕见病新药只要持续供应即可享有不超过7年的市场独占权,同样在此期间不再批准上市品种。
国家医保局在解决罕见病药品支付问题方面也取得进展。 2022年医保目录调整中,7种罕见病药品纳入医保谈判,部分产品价格下调90%以上。 据2023年1月央视新闻报道,我国医保目录包含52种罕见病药物,覆盖27种罕见病。
国内某药企不愿透露姓名的人士告诉澎湃新闻,2018年,五部委联合下发了《关于发布第一批罕见病目录的通知》。 这份文件被业内认为给罕见病诊疗敲响了警钟。 此后,医保向罕见病倾斜,包括本次目录扩容,可见国家政策在该领域的持续发力。 衷心希望看到更多的罕见病,看到更多的罕见病患者。 需求得到重视并得到有效解决。
另一位关注罕见病的国内药企人士此前对记者表示,新药研发是“九死一生”,风险极高,尤其是罕见病药物。 很多药企其实都有研究罕见病的想法,但很多时候他们不知道这样的产品未来在中国是否有真正的前景,所以不敢真正去做。 可见,近年来,对于罕见病的政策支持力度越来越大。 相信会鼓励更多的力量参与解决罕见病面临的问题。
多个已上市或在研罕见病适应症已纳入罕见病目录
据弗若斯特沙利文预计,2020年国内罕见病药物市场规模将达到13亿美元,2030年可能增长至259亿美元。千亿赛道吸引了医药巨头和一大批新兴生物制药企业。
从最新的《第二批罕见病目录》来看,86种罕见病包括神经母细胞瘤、神经纤维瘤病、腱鞘巨细胞瘤、泛发性脓疱性银屑病等,涉及肿瘤、皮肤、风湿、免疫、内分泌、肿瘤等多个疾病领域,其中一些有治疗罕见疾病的药物或处于临床研究后期。
再鼎医药(9688.HK)管线产品5个适应症入选罕见病目录,包括慢性炎症性脱髓鞘性多发性神经根神经病(CIDP)、胃肠道间质瘤(GIST)、胶质母细胞瘤(GBM)、恶性胸膜间皮瘤(MPM)、天疱疮, ETC。
再鼎医药对澎湃新闻表示,随着这份罕见病目录的发布,相信在相关政策的引导下,未来将会不断涌现更多突破性的罕见病解决方案。 保障罕见病治疗不仅是医学问题,也是急需解决的社会问题。 “疾病很罕见,但治疗不应罕见。” 我们期待全社会共同努力,改善和解决我国罕见病患者的治疗困难,加快我国罕见病事业的发展。
和宇药业(2256.HK)首款产品匹米克替尼(ABSK021)的适应症之一是腱鞘巨细胞瘤,已进入罕见病目录。 2023年半年报显示,该药已在中国、美国、欧洲同步启动全球III期研究。
和宇药业向澎湃新闻记者介绍,虽然腱鞘巨细胞瘤是一种罕见病,但我国每年新增患者6万至7万人,现有患者数为30万至40万。 国内患者的数量并不少见。 该适应症入选罕见病目录,有望加快产品审批进程,加快上市时间,让腱鞘巨细胞瘤患者尽快受益。
全身性脓疱型银屑病被列入罕见病名单。 澎湃新闻记者注意到,国内针对这种罕见疾病的产品已经上市或正在研发中。 今年5月,知名跨国制药公司勃林格殷格翰宣布,用于治疗广泛性脓疱型银屑病(GPP)的创新靶向生物制剂佩索珠单抗注射液已开始正式应用于临床,用于治疗该疾病。 进入精准瞄准时代。
华海药业(600521)旗下华泰正在研发泛发性脓疱型银屑病相关药物。 2023年半年报显示,该药代号HB0034,目前临床重点开发适应症为泛发性脓疱型银屑病。 奥泰在新西兰和中国进行的III期临床研究表明,HB0034在健康志愿者和GPP患者中安全且耐受性良好。 目前,HB0034已向美国食品药品监督管理局(FDA)提交孤儿药认定申请。 同时,华泰还与国家药品审评中心(CDE)保持积极沟通,加快相关临床工作的推进。
神经纤维瘤病也被列入罕见疾病名单。 今年5月,阿斯利康中国宣布,司美替尼硫酸氢胶囊在中国正式获批用于治疗3岁及以上有症状且无法治疗神经纤维瘤病的患者。 对于I型神经纤维瘤病儿童丛状神经纤维瘤的手术治疗。对于《第二批罕见病目录》的意义,阿斯利康告诉澎湃新闻,该目录的出台体现了国家完善罕见病诊疗和保障体系的决心。罕见疾病。 目录的推出可以进一步增进对罕见病的认识。 加强罕见病诊疗能力,促进罕见病药物研发和可及性,造福更多罕见病患者。 阿斯利康也将继续加快罕见病创新药物的推出,联合产业生态,造福更多罕见病患者。
上述不愿透露姓名的药企人士也指出,对于药企来说,罕见病药物的研发是“更温暖的创新”。 当前,进一步解决罕见病药品纳入医保准入后的“最后一公里”问题,确保罕见病患者用得上药品,还有很长的路要走。
现在送你60元福利红包,直接提现,无需任何技巧~~~快来参加活动吧!


海量信息、精准解读,尽在新浪财经APP
搜虎网转载此文目的在于传递更多信息,不代表本网的观点和立场。文章内容仅供参考,不构成投资建议。投资者据此操作,风险自担。
-

加油站盗油事件调查:揭露违法行为 严查维权保消费
据统计,我国机动车保有量已达4.35亿辆,新注册登记汽车更是连续十年以每年超过20...
-

贾樟柯新作风流一代在戛纳电影节引发热议,深度解析
讯 www.yule.com.cn 法国当地时间5月18日,第77届戛纳电影节于首周末举办贾樟...
-

深度解读安徽淮南武王墩一号墓的青铜鼎:楚国历史的
昨天,国家文物局发布安徽淮南武王墩一号墓考古发掘以及文物保护重要成果,墓主人...
-

深度剖析:去库存是房地产市场复苏的关键环节
本周五,楼市迎来诸多利好,四项重磅政策同时出炉,包括购房首付比例下调、公积金贷...
-

河南中原消费金融拟发行20亿元金融债 扩大资金来
了2024年金融债券(第一期),发行规模为10亿元;兴业消费金融分别发行了三期金融债...
 Copyright ? 2017-2018
Copyright ? 2017-2018
Copyright ? 2017 搜虎网 www.xmsouhu.com 版权所有 搜虎网